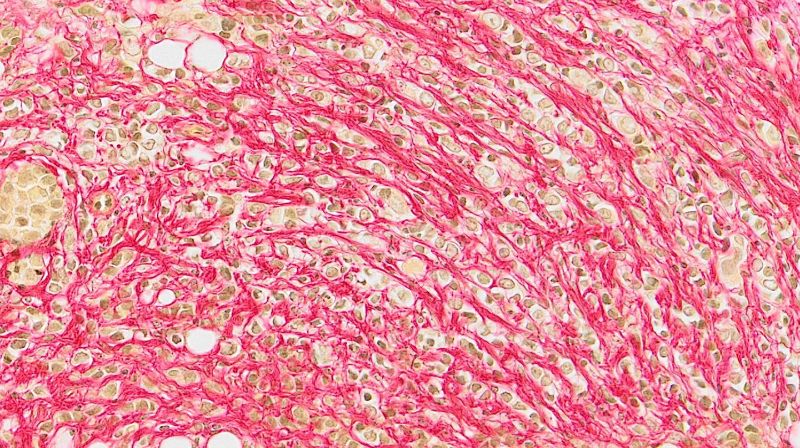
Modell einer besonderen Art von Brustkrebst
Das invasive lobuläre Karzinom (ILC) ist eine Form von Brustkrebs, die in den milchproduzierenden Drüsen (Läppchen) der Brust beginnt. Es macht 10-15 % aller Brustkrebsfälle aus, hat ein hohes Risiko für ein späteres Wiederauftreten, einzigartige Metastasenstandorte, eine hohe Empfindlichkeit gegenüber Hormonen, unvorhersehbare Reaktionen auf Therapien, eine einzigartige Histopathologie, eine ausgeprägte Biologie und ist resistent gegen Chemotherapie. Mehr als 90 % der ILC-Tumoren enthalten ausserdem Östrogenrezeptoren, was bedeutet, dass sie Hormonsignale vom Körper empfangen können, z. B. Östradiol, die ihr Wachstum und ihre Metastasierung ankurbeln können.
Trotz alledem ist ILC im Vergleich zu anderen Brustkrebsarten relativ wenig erforscht, so dass nur sehr wenige Modelle entwickelt wurden, um ihn zu untersuchen. Grund dafür ist die geringere Inzidenz von ILC im Allgemeinen, aber auch, weil sich ILC-Tumore nicht für das Wachstum in Kulturen oder in Mäusen eignen, was für die Entwicklung von Modellen entscheidend ist.
Jetzt haben Wissenschaftlerinnen der EPFL die Einschränkungen des ILC erfolgreich überwunden und ein Xenotransplantationsmodell für ihn entwickelt, das den Tumor mit hoher Genauigkeit simuliert. Die Forschenden, unter Leitung des EPFL-Forschers George Sflomos im Labor von Professor Cathrin Brisken, transplantierten zwei von ILC abgeleitete metastatische Brustkrebs-Zelllinien sowie frisch resezierte ILC-Tumore von Patientinnen direkt in die Milchgänge von immunschwachen Mäusen. Die Studie wurde jetzt in EMBO Molecular Medicine veröffentlicht.
Der Ansatz erlaubte es den Forschenden, eine Reihe von In-vivo-Modellen von lobulärem Brustkrebs zu entwickeln. Besonders wichtig ist, dass diese experimentellen ILC-Tumore die Östrogenrezeptor-Expression sowie ihre Ansprechbarkeit auf Östradiol beibehalten, die ILC-Tumore typischerweise aufweisen. «Die Proben bewahren die histomorphologischen Aspekte und die eigentümlichen metastatischen Muster von ILC. Die Ergebnisse sind besonders wichtig für die Untersuchung der ILC-Metastasierung, die in erster Linie für die krebsbedingte Sterblichkeit bei ILC verantwortlich ist», sagt George Sflomos, Erstautor der Studie.
Die Modelltumore enthüllten auch einige Geheimnisse der ILC-Biologie. Sie scheinen ähnliche Besonderheiten in der extrazellulären Matrix zu haben, wie ihre intrinsische Fähigkeit, Elastin, Kollagene und das kollagenmodifizierende Enzym LOXL1 zu produzieren. Als die Forschenden also alle LOX-Enzyme blockierten, sahen sie einen Rückgang des Primärtumorwachstums, der Metastasierung und der Östrogenrezeptor-Signalisierung. «LOXL1 erwies sich als essentiell für die in vivo-Tumorprogression, was darauf hindeutet, dass die gezielte Beeinflussung der Mikroumgebung des ILC-Tumors ein vielversprechender therapeutischer Ansatz sein kann, der neue Horizonte in der Biologie der Krankheit eröffnet, von denen ILC-Patientinnen profitieren würden», sagt Sflomos.
«Dieses Modell liefert uns die ersten tiefen Einblicke in den häufigsten der Brustkrebs-Subtypen, den Östrogenrezeptor-positiven Brustkrebs-Subtyp», sagt Cathrin Brisken. «Diese experimentelle Modellierung von ILC hilft, für die Krankheit spezifische molekulare Mechanismen zu identifizieren und in naher Zukunft neue therapeutische Ziele zu entdecken.»