Ein tiefer Einblick in das Fortschreiten der Parkinson-Krankheit
Die Parkinson-Krankheit ist eine komplexe neurodegenerative Erkrankung, die zum Abbau bestimmter Arten von Neuronen im Gehirn führt und eine Reihe von motorischen und nicht-motorischen Symptomen hervorruft. Derzeit leben schätzungsweise mehr als 10 Millionen Menschen in der Welt mit der Parkinson-Krankheit, der zweithäufigsten neurodegenerativen Erkrankung nach Alzheimer. Es wird erwartet, dass diese Zahl bis zum Jahr 2040 auf 14 Millionen ansteigt, was als Parkinson-Pandemie bezeichnet wird.
Eines der wichtigsten Ereignisse bei der Parkinson-Krankheit ist die Anhäufung eines Proteins namens Alpha-Synuclein in den Neuronen. Diese Anhäufung stört die normale Funktion der Zellen, was zu den Symptomen der Parkinson-Krankheit und anderer Störungen führt, und entwickelt sich zu Aggregaten, die Lewy-Körperchen genannt werden.
In einer neuen Studie haben Forschende aus zwei Labors der EPFL ihr Fachwissen gebündelt, um zu untersuchen, wie Alpha-Synuclein die Stoffwechselprozesse in den Neuronen stört. Die Studie ist eine wirklich interdisziplinäre Zusammenarbeit zwischen der Bertarelli-Plattform für Gentherapie von Bernard Schneider und der Gruppe von Anders Meibom an der EPFL, mit Unterstützung der Bioelectron Microscopy Core Facility der EPFL.
Die Forschenden setzten hochmoderne Bildgebungsverfahren ein, darunter ein Analyseinstrument namens NanoSIMS (Nanoscale Secondary Ion Mass Spectrometry). NanoSIMS ist eine «Ionen-Mikrosonde», die eine hohe räumliche Auflösung (50-150 nm), eine hochauflösende Massenspektrometrie und eine hohe analytische Empfindlichkeit miteinander verbindet, so dass subzelluläre Karten des Stoffwechselgeschehens mit extremer Empfindlichkeit erstellt werden können. Meiboms Labor an der EPFL hat NanoSIMS bereits für eine Reihe von ökologischen und geologischen Studien eingesetzt.
In dieser Studie kombinierten die Forschenden NanoSIMS mit der Markierung stabiler Isotope, um Isotopenvariationen in Geweben mit hoher Auflösung sichtbar zu machen und so Einblicke in die Stoffwechselaktivität einzelner Zellkompartimente und Organellen zu erhalten. Sie kombinierten dies mit der Elektronenmikroskopie, um mehr Informationen aus biologischen Proben zu «sehen».
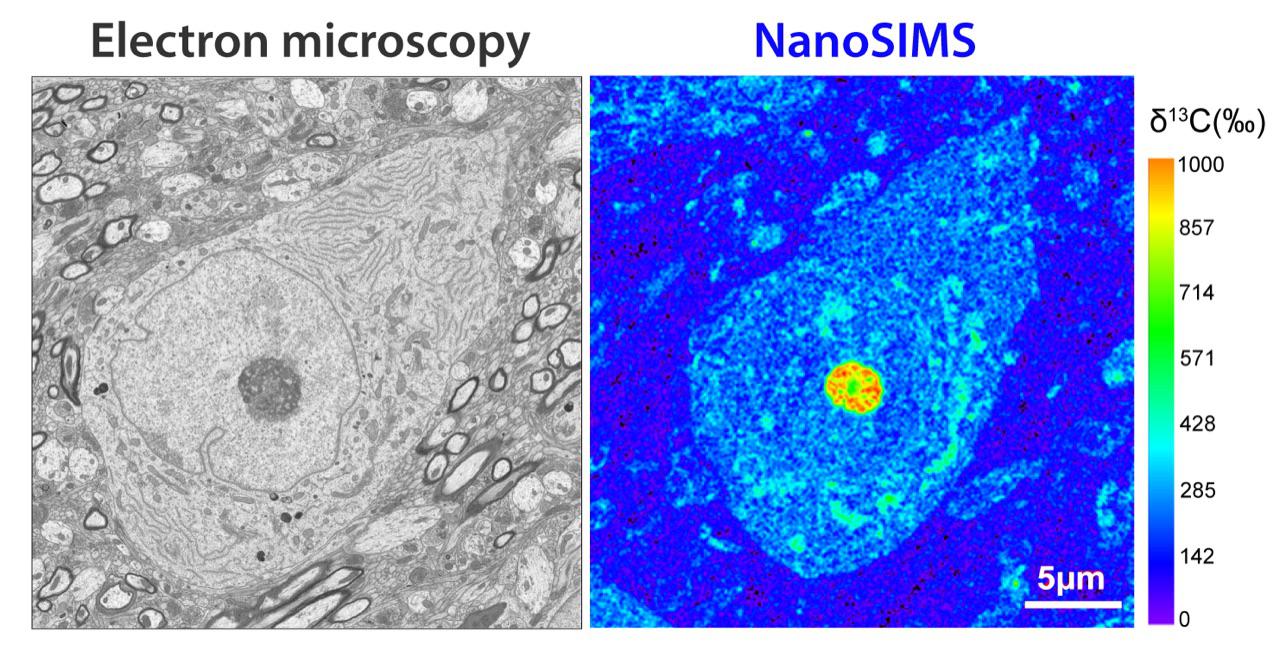
Ein elektronenmikroskopisches Bild mit der entsprechenden NanoSIMS-13C-Karte. Entnommen aus Spataro et al. 2023.
Um die Parkinson-Krankheit zu modellieren, verwendete das Team genetisch veränderte Ratten, bei denen menschliches Alpha-Synuclein in einer Gehirnhälfte überexprimiert wurde, während die andere Hemisphäre als Kontrolle gesund blieb. Beim Vergleich der Neuronen, die Alpha-Synuclein überexprimieren, mit denen in der Kontrollhälfte entdeckten die Wissenschaftler erhebliche Veränderungen in der Art und Weise, wie Kohlenstoffmoleküle in den Neuronen aufgenommen und verarbeitet werden.
Einer der bemerkenswertesten Befunde war die Auswirkung von Alpha-Synuclein auf den Umsatz von Kohlenstoff in den Neuronen. Neuronen, die Alpha-Synuclein überexprimieren, wiesen einen erhöhten Gesamtumsatz an Makromolekülen auf, was darauf hindeutet, dass die Anhäufung von Alpha-Synuclein zu erhöhten metabolischen Anforderungen an diese Zellen führen kann.
In der Studie wurden auch Veränderungen in der Verteilung des Kohlenstoffs zwischen verschiedenen Zellkompartimenten wie dem Zellkern und dem Zytoplasma festgestellt, die möglicherweise durch die Interaktion von Alpha-Synuclein mit DNA und Histonen beeinflusst werden.
Die durch Alpha-Synuclein verursachten Stoffwechselstörungen scheinen auch bestimmte Organellen zu beeinträchtigen: In den Mitochondrien wurden beispielsweise abnorme Muster des Kohlenstoffeinbaus und -umsatzes festgestellt, was mit früheren Studien übereinstimmt, die zeigten, dass Alpha-Synuclein die Funktion der Mitochondrien beeinträchtigt. Auch der Golgi-Apparat, der für den zellulären Transport und die Kommunikation zuständig ist, wies Stoffwechseldefekte auf, die wahrscheinlich darauf zurückzuführen sind, dass Alpha-Synuclein die Kommunikation zwischen den Organellen gestört hat.
«Diese Studie zeigt das Potenzial der NanoSIMS-Technologie, Stoffwechselveränderungen im Gehirn mit einer noch nie dagewesenen Auflösung auf subzellulärer Ebene aufzudecken», sagt Bernard Schneider, «Sie gibt uns ein Werkzeug an die Hand, um frühe pathologische Veränderungen zu untersuchen, die in anfälligen Neuronen als Folge der Anhäufung von Alpha-Synuclein auftreten, ein Mechanismus, der direkt mit der Parkinson-Krankheit in Verbindung steht.»
